Cos’è lo Pneumotorace Spontaneo? Perché è un grave problema clinico e come si effettua la diagnosi? Quante tipologie si conoscono?
Lo pneumotorace spontaneo rappresenta un problema clinico comune, che può colpire i polmoni in qualsiasi momento. Viene descritta una panoramica delle informazioni pertinenti e aggiornate su epidemiologia, fisiopatologia e causa / e di pneumotorace spontaneo (primario e secondario).
Lo pneumotorace è definito come la presenza di aria nello spazio pleurico. Sebbene le pressioni intrapleuriche siano negative durante la maggior parte del ciclo respiratorio, l’aria non entra nello spazio pleurico perché la somma di tutte le pressioni parziali dei gas nel sangue capillare è in media di soli 93,9 kPa (706 mmHg).
Quindi, il movimento netto dei gas dal sangue capillare nello spazio pleurico richiederebbe pressioni pleuriche inferiori a -54 mmHg (cioè inferiori a -36 cmH2O), che raramente si verificano in circostanze normali.
Quindi, se è presente aria nello spazio pleurico, deve essersi verificato uno dei tre eventi:
- comunicazione tra spazi alveolari e pleura;
- comunicazione diretta o indiretta tra l’atmosfera e lo spazio pleurico;
- presenza di organismi che producono gas nello spazio pleurico.
Da un punto di vista clinico, lo pneumotorace è classificato come spontaneo (nessun fattore precipitante evidente presente) e non spontaneo.
Lo pneumotorace spontaneo primario (PSP) è definito come la presenza spontanea di aria nello spazio pleurico in pazienti senza malattia polmonare sottostante clinicamente evidente.
Pneumotorace spontaneo primario.
Il PSP ha un’incidenza da 7,4 a 18 casi (incidenza aggiustata per età) per 100.000 abitanti ogni anno nei maschi e da 1,2 a 6 casi per 100.000 abitanti ogni anno nelle femmine.
Il PSP si verifica tipicamente in soggetti alti e magri. Altri fattori di rischio sono il sesso maschile e il fumo di sigaretta. Contrariamente alla credenza popolare, la PSP si manifesta tipicamente a riposo; evitare l’esercizio, quindi, non dovrebbe essere raccomandato per prevenire le recidive. Fattori precipitanti possono essere i cambiamenti della pressione atmosferica (che possono spiegare il raggruppamento spesso osservato della PSP) e l’esposizione alla musica ad alto volume.
Quasi tutti i pazienti con PSP riferiscono un improvviso dolore toracico omolaterale, che di solito si risolve spontaneamente entro 24 ore. Può essere presente dispnea, ma di solito è lieve. L’esame obiettivo può essere normale nei piccoli pneumotoraci. Negli pneumotoraci più grandi, i suoni del respiro e il fremito tattile sono tipicamente ridotti o assenti e la percussione è iper-risonante. L’ipotensione, la tachipnea, la tachicardia e la cianosi in rapida evoluzione dovrebbero far sorgere il sospetto di pneumotorace tensivo, che è, tuttavia, estremamente raro nella PSP.
Diagnosi di PSP.
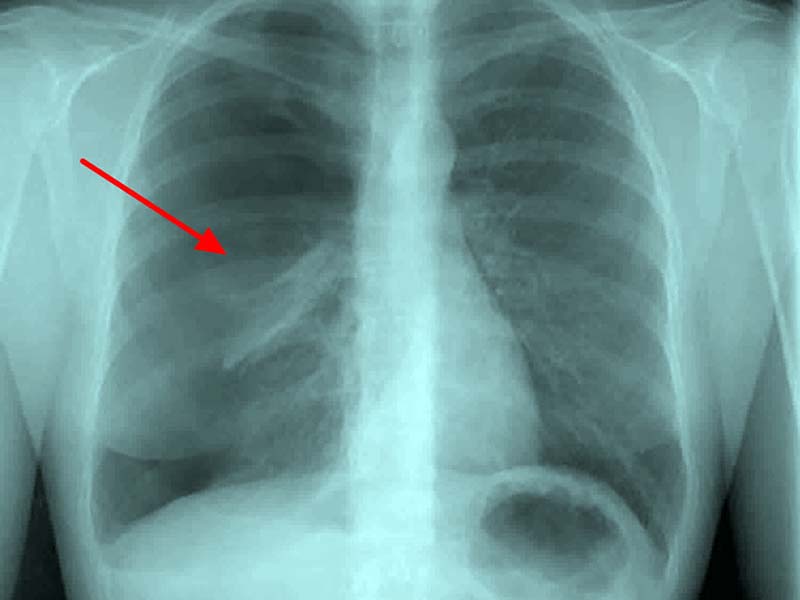
La diagnosi può essere confermata nella maggior parte dei casi su una radiografia del torace verticale posteroanteriore (PA), che consente anche una stima delle dimensioni dello pneumotorace con buona precisione [9]. Nei casi con una piccola PSP, può essere necessaria la tomografia computerizzata (TC) per diagnosticare la presenza di aria pleurica. Le radiografie del torace espiratorie di routine sono inutili.
È importante rendersi conto che uno spostamento controlaterale della trachea e del mediastino è un fenomeno del tutto normale nello pneumotorace spontaneo e per nulla suggestivo per lo pneumotorace tensivo; questa osservazione non dovrebbe quindi in alcun modo influenzare le strategie di trattamenti.
Patogenesi.
L’esatta patogenesi del verificarsi spontaneo di una comunicazione tra gli spazi alveolari e la pleura rimane sconosciuta. La maggior parte degli autori ritiene che la rottura spontanea di una bolla subpleurica, o di una bolla, sia sempre la causa della PSP, ma sono disponibili spiegazioni alternative.
Sebbene la maggior parte dei pazienti con PSP, compresi i bambini, presenti vesciche o bolle, non è chiaro quanto spesso queste lesioni siano effettivamente il sito di perdita d’aria.
Solo una minoranza di blebs è effettivamente rotta al momento della toracoscopia o dell’intervento chirurgico, mentre spesso sono presenti altre lesioni (“porosità pleurica”: aree di cellule mesoteliali interrotte a livello della pleura viscerale, sostituite da uno strato elastofibrotico infiammatorio con maggiore porosità, che consente la fuoriuscita di aria nello spazio pleurico).
Quest’ultimo fenomeno può spiegare gli alti tassi di recidiva fino al 20% della sola bullectomia (senza pleurodesi associata) come terapia. Lo sviluppo di blebs, bolle e aree di porosità pleurica può essere collegato a una varietà di fattori, tra cui infiammazione delle vie aeree distali, predisposizione ereditaria, anomalie anatomiche dell’albero bronchiale, fisionomia ectomorfa con più pressioni intrapleuriche negative e ischemia apicale agli apici, basso indice di massa corporea e restrizione calorica e tessuto connettivo anormale.
Il ruolo dell’aumento delle concentrazioni plasmatiche di alluminio nella patogenesi della PSP rimane irrisolto.
Queste lesioni possono, quindi, predisporre alla PSP se combinate con fattori precipitanti (in gran parte sconosciuti); blebs e bullae infatti si verificano anche fino al 15% dei soggetti normali. Nuove tecniche come la toracoscopia con autofluorescenza potenziata con fluoresceina o la toracoscopia a infrarossi possono fare più luce su questo problema e possono essere utili per l’individuazione delle aree colpite durante la toracoscopia o l’intervento chirurgico. Dovrebbe essere chiaro, tuttavia, che ogni intervento terapeutico con lo scopo di prevenire le recidive di PSP dovrebbe includere una tecnica di pleurodesi, con o senza un intervento a livello del parenchima polmonare.
Pneumotorace Spontaneo Secondario..
Una moltitudine di disturbi respiratori è stata descritta come causa di pneumotorace spontaneo. Le patologie sottostanti più frequenti sono la broncopneumopatia cronica ostruttiva con enfisema, fibrosi cistica, tubercolosi, cancro ai polmoni e polmonite da Pneumocystis carinii associata all’HIV, seguite da patologie più rare ma “tipiche”, come linfangioleiomiomatosi e istiocitosi X.
Poiché la funzione polmonare in questi pazienti è già compromessa, lo pneumotorace spontaneo secondario (SSP) si presenta spesso come una malattia potenzialmente pericolosa per la vita, che richiede un’azione immediata, in contrasto con la PSP, che è più un fastidio che una condizione pericolosa. L’incidenza generale è quasi simile a quella della PSP.
A seconda della malattia sottostante, il picco di incidenza di SSP può verificarsi più tardi nella vita, ad es. 60-65 anni di età nella popolazione di enfisema.
Nella SSP, la dispnea è la caratteristica clinica più importante; Possono essere presenti anche dolore toracico, cianosi, ipossiemia e ipercapnia, che talvolta provocano insufficienza respiratoria acuta. La diagnosi è confermata da una radiografia del torace PA; nell’enfisema bolloso, la diagnosi differenziale con una bolla gigante può essere difficile, richiedendo la conferma TC.
Come nella PSP, l’aria può entrare nello spazio pleurico attraverso vari meccanismi: rottura alveolare diretta (come nell’enfisema o nella polmonite necrotica), attraverso l’interstizio polmonare, o all’indietro attraverso il fascio broncovascolare e la pleura mediastinica (pneumomediastino).
I tassi di recidiva di solito sono più alti rispetto a quelli per la PSP, fino all’80% dei casi, come si osserva nella fibrosi cistica.
Servizio di M. Noppen – European Respiratory Review 2010 19: 217-219; DOI: 10.1183/09059180.00005310
Traduzione: Angelo Riky Del Vecchio – Direttore AssoCareNews.it
Leggi anche:
Polmoni: organi fondamentali per gli scambi gassosi e per la sopravvivenza dell’individuo.
Bibliografia.
- Jantz MA, Anthony VB. Pathophysiology of the pleura. Respiration 2008; 75: 121–133.CrossRefPubMedGoogle Scholar;
- Noppen M, Schramel F. Pneumothorax. Eur Respir Mon 2002; 22: 279–296.Google Scholar;
- Baumann MH, Noppen M. Pneumothorax. Respirology 2004; 9: 157–164.CrossRefPubMedGoogle Scholar;
- Bense L, Eklund G, Wilman LG. Smoking and the increased risk of contracting spontaneous pneumothorax. Chest 1987; 92: 1009–1012.CrossRefPubMedGoogle Scholar;
- Melton LJ, Hepper NGG, Offord KP. Incidence of spontaneous pneumothorax in Olmsted County, Minnesota: 1050–74. Am Rev Respir Dis 1979; 120: 1379–1382.PubMedGoogle Scholar;
- Bense L, Wilman LG, Hedenstierna G. Onset of symptoms in spontaneous pneumothorax: correlations to physical activity. Eur J Respir Dis 1987; 71: 181–186.PubMedGoogle Scholar;
- Alifano M, Forti Parri SN, Bonfanti B, et al. Atmospheric pressure influences the risk of pneumothorax: beware of the storm!. Chest 2007; 131: 1877–1882.CrossRefPubMedGoogle Scholar;
- Noppen M, Verbanck S, Harvey J, et al. Music: a new cause of primary spontaneous pneumothorax. Thorax 2004; 59: 722–724.Abstract/FREE Full TextGoogle Scholar;
- Noppen M, Alexander P, Driesen P, et al. Quantification of the size of primary spontaneous pneumothorax: accuracy of the Light index. Respiration 2001; 68: 396–399.CrossRefPubMedGoogle Scholar;
- Bradley M, Willams C, Walshaw MJ. The value of routine expiratory films in the diagnosis of pneumothorax. Arch Emerg Med 1991; 8: 115–116.PubMedGoogle Scholar;
- Light RW. Management of spontaneous pneumothorax. Am Rev Respir Dis 1993; 148: 245–248.CrossRefPubMedGoogle Scholar;
- Sahn SA, Heffner JE. Spontaneous pneumothorax. N Engl J Med 2000; 342: 868–874.CrossRefPubMedGoogle Scholar;
- Noppen M. Con: blebs are not the cause of primary spontaneous pneumothorax. J Bronchol 2002; 9: 319–325.CrossRefGoogle Scholar;
- Guimaraes CV, Donnely LF, Warner BW. CT findings for blebs and bullae in children with spontaneous pneumothorax and comparison with findings in normal age-matched controls. Pediatr Radiol 2007; 37: 879–884.CrossRefPubMedGoogle Scholar;
- Amjadi K, Alvarez GG, Vanderhelst E, et al. The prevalence of blebs and bullae among young healthy adults: a thoracoscopic evaluation. Chest 2007; 132: 1140–1145.CrossRefPubMedGoogle Scholar;
- Bense L, Lewander R, Eklund G, et al. Non-smoking, non-alpha 1 antitrypsin deficiency-induced emphysema in nonsmokers with healed spontaneous pneumothorax, identified by computed tomography of the lungs. Chest 1993; 103: 433–438.CrossRefPubMedGoogle Scholar;
- Lesur O, Delorme N, Fromaget JM, et al. Computed tomography in the etiologic assessment of idiopathic spontaneous pneumothorax. Chest 1990; 98: 341–347.CrossRefPubMedGoogle Scholar;
- Schramel F, Postmus PE, Vanderschueren RG. Current aspects of spontaneous pneumothorax. Eur Respir J 1997; 10: 1372–1379.Abstract/FREE Full TextGoogle Scholar;
- Randomsky JBH, Hartel W. Pleuraporositat beim idiopatischen spontanpneumothorax [Pleural porosity in idiopathic spontaneous pneumothorax]. Pneumologie 1989; 43: 250–253.PubMedGoogle Scholar;
- Masshof W, Hofer W. Zur pathologie der sogenannten idiopatischen spontanpneumothorax [Pathology of so-called idiopathic spontaneous pneumothorax]. Dtsch Med Wochenschr 1973; 98: 801–805.PubMedGoogle Scholar;
- Ohata M, Suzuki H. Pathogenesis of spontaneous pneumothorax. With special reference to the ultratsructure of emphysematous bullae. Chest 1980; 77: 771–776.CrossRefPubMedGoogle Scholar;
- Hatz RA, Kaps MF, Meimerakis G, et al. Long-term results after video-assisted thoracoscopic surgery for first-time and recurrent spontaneous pneumothorax. Ann Thorac Surg 2000; 70: 253–257.CrossRefPubMedGoogle Scholar;
- Korner H, Andersen KS, Stangeland L, et al. Surgical treatment of spontaneous pneumothorax by wedge resection without pleurodesis or pleurectomy. Eur J Cardiothorac Surg 1996; 10: 656–659.Abstract/FREE Full TextGoogle Scholar;
- Loubani M, Lynch V. Video-assisted thoracoscopic bullectomy and acromycin pleurodesis: an effective treatment for spontaneous pneumothorax. Respir Med 2000; 94: 888–890.CrossRefPubMedGoogle Scholar;
- Horio H, Nomori H, Kobayashi R, et al. Impact of additional pleurodesis in video-assisted thoracoscopic bullectomy for primary spontaneous pneumothorax. Surg Endosc 2002; 16: 630–634.CrossRefPubMedGoogle Scholar;
- Schramel F, Meyer CJ, Postmus PE. Inflammation as a cause of spontaneous pneumothorax and emphysema-like changes: results of bronchoalveolar lavage. Eur Respir J 1995; 8 Suppl. 19397s–Google Scholar;
- Morrison PJ, Lowry RC, Nevin NC. Familial primary spontaneous pneumothorax consistent with true autosomal dominant inheritance. Thorax 1998; 53: 151–152.AbstractGoogle Scholar;
- Bense L, Eklund G, Wiman LG. Bilateral bronchial anomaly. A pathogenetic factor in spontaneous pneumothorax. Am Rev Respir Dis 1992; 146: 513–516.PubMedGoogle Scholar;
- Fujino S, Inoue S, Tezuka N, et al. Physical development of surgically treated patients with primary spontaneous pneumothorax. Chest 1999; 116: 899–902.CrossRefPubMedGoogle Scholar;
- Withers JN, Fishback ME, Kiehl PV, et al. Spontaneous pneumothorax. Suggested etiology and comparison of treatment methods. Am J Surg 1964; 108: 772–776.CrossRefPubMedGoogle Scholar;
- Kawajami Y, Irie T, Kawashima K. Stature, lung height, and spontaneous pneumothorax. Respiration 1982; 43: 35–40.CrossRefPubMedGoogle Scholar;
- Coxson HO, Chan IHT, Mayo JR, et al. Early emphysema in patients with anorexia nervosa. Am J Respir Crit Care Med 2004; 170: 748–752.CrossRefPubMedGoogle Scholar;
- Neptune ER, Frischmeyer PA, Arking DE, et al. Dysregulation of TGF-beta activation contributes to pathogenesis in Marfan syndrome. Nat Genet 2003; 33: 407–411.CrossRefPubMedGoogle Scholar;
- Loeys BL, Matthys DM, De Paepe AM. Genetic fibrillinopathies: new insights in molecular diagnosis and clinical management. Acta Clin Belg 2003; 58: 3–11.PubMedGoogle Scholar;
- Han S, Sakinci U, Kose SK, et al. The relationship between aluminium and spontaneous pneumothorax: treatment, prognosis, follow up. Interact Cardiovasc Thorac Surg 2004; 3: 79–82.Abstract/FREE Full TextGoogle Scholar;
Leo F, Venissac N, Drici MD, et al. Aluminium and spontaneous pneumothorax. A suggestive but unconfirmed hypothesis. Interact Cardiovasc Thorac Surg 2005; 4: 21–22.Abstract/FREE Full TextGoogle Scholar; - Noppen M, Dekeukeleire T, Hanon S, et al. Fluorescein enhanced autofluorescence thoracoscopy in primary spontaneous pneumothoarx and normal subjects. Am J Respir Crit Care Med 2006; 174: 26–30.CrossRefPubMedGoogle Scholar;
- Gotoh M, Yamamoto Y, Igai H, et al. Clinical application of infrared thoracoscopy to detect bullous or emphysematous lesions of the lung. J Thorac Cardiovasc Surg 2007; 134: 1498–1501.CrossRefPubMedGoogle Scholar;
- Noppen M, Baumann MH. Pathogenesis and treatment of primary spontaneous pneumothorax: an overview. Respiration 2003; 70: 431–438.CrossRefPubMedGoogle Scholar;
- Bourgouin P, Cousineau G, Lemire P, et al. Computed tomography used to exclude pneumothorax in bullous lung disease. J Can Assoc Radiol 1985; 36: 341–342.PubMedGoogle Scholar;
- Edenborough FB, Hussain I, Stableforth DE. Use of a Heimlich flutter valve for pneumothorax in cystic fibrosis. Thorax 1994; 49: 1178–1179.Abstract/FREE Full TextGoogle Scholar.



[…] Pneumotorace Spontaneo: cause, sintomi e tipologie. proviene da AssoCareNews.it – Quotidiano Sanitario […]
[…] Pneumotorace Spontaneo: cause, sintomi e tipologie. proviene da AssoCareNews.it – Quotidiano Sanitario […]
[…] Pneumotorace Spontaneo: cause, sintomi e tipologie. proviene da AssoCareNews.it – Quotidiano Sanitario […]