Tra i diversi trattamenti oggi utilizzati nel Wound Care, la terapia a pressione negativa rappresenta una soluzione apprezzata e utile nei casi in cui la ferita non raggiunga risultati di guarigione significativi.
La cura della lesione in ambiente a pressione subatmosferica (o negativa), viene denominato in vari modi:
- NPWT (Negative Pressure Wound Therapy);
- TPN (Terapia Pressione Negativa);
- NPT (negative pressure therapy), tutti sinonimi corretti.
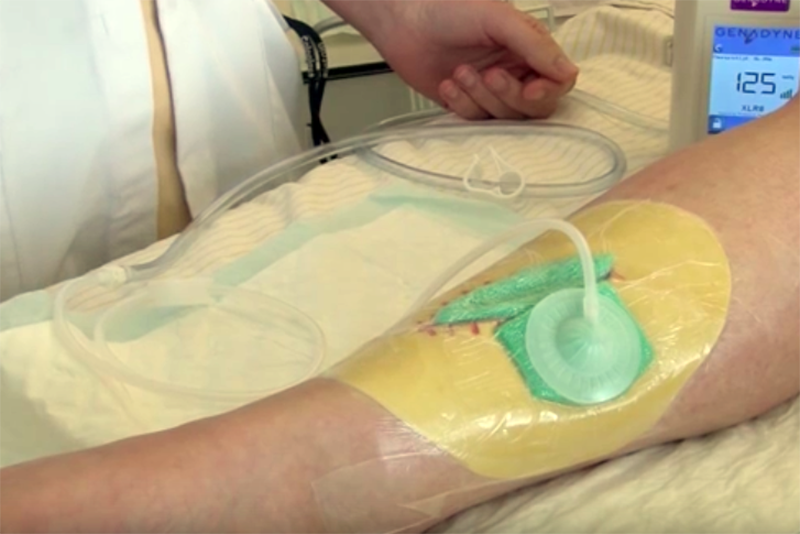
Pressione negativa è un termine che designa una pressione inferiore a quella atmosferica normale. A temperatura ambiente ed a livello del mare, un determinato volume di aria contiene molecole che si muovono a caso ed esercitano una forza che corrisponde alla pressione atmosferica normale di 760 mmHg. Per ottenere una pressione negativa basta allontanare le molecole gassose dall’area interessata (per es. il sito della ferita) usando, ad esempio, una pompa aspirante.Un riempimento in schiuma o garza è applicato nello spazio della lesione, un tubicino è inserito nella ferita, il tutto è sigillato con una pellicola adesiva. La pellicola gas-permeabile permette lo scambio gassoso e allo stesso tempo protegge la ferita. Il tubicino convoglia la pressione negativa al sito lesionale e si genera un effetto ventosa attorno all’applicazione della schiuma o della garza. Il cambio della schiuma è raccomandato ogni 48 ore per gli adulti e giornalmente per adolescenti e bambini. L’impiego clinico della pressione negativa risale a migliaia di anni fa. Essa è stata usata per la prima volta nella medicina cinese in aggiunta alle tecniche di agopuntura, dopo che è stato osservato come provochi iperemia. Più tardi, nel 1841, Junod adottò il metodo usando coppette di vetro riscaldate applicate alla cute del paziente per “stimolare la circolazione”. Con il raffreddarsi dell’aria, all’interno delle coppette si creava una pressione subatmosferica che provocava iperemia. Da allora sono state registrate numerose varianti della TNP therapy. Nel 1993, Fleischmann et al hanno applicato la pressione topica negativa a ferite tramite una medicazione in schiuma per un periodo prolungato, allo scopo di promuovere la granulazione e la riparazione tessutale, in pazienti con fratture aperte. Hanno potuto così osservare un’efficiente detersione della ferita senza infezioni ossee (sebbene uno dei pazienti abbia subito un’infezione dei tessuti molli). Nei loro primi studi, la pressione negativa all’interno della ferita è stata ottenuta tramite una semplice unità di aspirazione murale o con aspiratori portatili per chirurgia.
Questi apparati tuttavia hanno comportato problemi pratici in termini di raggiungimento, controllo e mantenimento dei livelli desiderati di pressione negativa. I ricercatori Morykwas e Argenta hanno disegnato una serie di studi su animali, usando la TNP therapy con una medicazione in schiuma PU che fungeva da interfaccia fra la superficie della ferita e la fonte del vuoto. La schiuma si è rivelata un elemento essenziale ed ha stimolato lo sviluppo da parte di Kinetic Concepts Inc. di un sistema commerciale (il sistema vacuum assisted closure [VAC]). La medicazione in schiuma PU, dotata di una struttura regolare di fori di grandi dimensioni (400–600 μm), è parte integrante del sistema e consente una distribuzione uniforme della pressione su tutta la superficie della ferita. Inoltre, il volume della schiuma si riduce se sottoposto a pressione, provocando così lo stiramento delle cellule, la contrazione della ferita e l’eliminazione dei fluidi. Più recentemente la concorrenza ha sviluppato alcune varianti di questo sistema, che però non prevedono l’uso di schiume.
Durante la cura a pressione negativa il letto di ferita viene sottoposto a tre attività principali:
- Rimozione del tessuto devitalizzato in eccesso (essudato, slough, materiali infetti).
- Contrazione della schiuma e conseguente riavvicinamento dei margini della ferita.
- Induzione di microdeformazioni nei tessuti della ferita, stimolando la proliferazione e accelerazione della guarigione della ferita.
I principali obiettivi di questo tipo di trattamento sono dunque:
- Rimuovere l’essudato in eccesso che riduce l’efficacia della terapia, e ritarda la guarigione.
- Stimolare il miglioramento del letto di ferita, prima della chiusura chirurgica o l’innesto di un trapianto cutaneo.
- Ristabilire la vascolarizzazione del letto della ferita e o favorire la formazione di tessuto di granulazione.
- Promuovere il progredire della guarigione quando le medicazioni tradizionali non danno
risultati positivi.
L’uso della NPWT è indicato in molti tipi di ferite acute e croniche e può essere presa in considerazione quando la ferita:
- non progredisce verso la guarigione nei tempi previsti, per esempio quando la contrazione dei margini della ferita avviene con troppa lentezza con le cure standard;
- produce una quantità eccessiva di essudato, difficile da trattare.
La NPWT permette una riduzione dei cambi di medicazione, quindi un risparmio sia per utilizzo improprio ed eccessivo di medicazioni avanzate, sia per il tempo di assistenza infermieristica impiegato; è localizzata in un punto disagevole oppure ha una dimensione tale da rendere problematica un’adeguata sigillatura con le medicazioni tradizionali; richiede una riduzione delle dimensioni prima di procedere ad una chiusura chirurgica.
L’utilizzo della TPN è controindicato in queste tipologie di ferite e o condizioni (FDA 2011):
- tessuto necrotico con presenza di escara;
- osteomieliti non trattate;
- fistole non enteriche e non esplorate (in questo caso si consiglia una radiografia o ecografia dei tessuti molli di controllo per visionare l’entità della tunnellizzazione);
- esposizione importante di osso (se presente una minima esposizione ossea favorire prima la ricrescita del tessuto con medicazioni avanzate e poi rivalutare per riposizionamento della TPN);
- lesioni neoplastiche;
- esposizione di vasi;
- esposizione di nervi;
- esposizione di anastomosi;
- esposizione di organi.
La TPN va interrotta quando non è evidente un risultato clinico dopo tre settimane di trattamento; compare dolore o disconfort, intolleranza, effetti collaterali riferibili alla terapia .
Per ottenere un’adeguata guarigione delle ferite bisogna innanzitutto effettuare un’efficiente cura del sito leso, che si può riassumere brevemente in:
- pulizia e o detersione;
- debridement – rimozione del tessuto morto;
- uso di medicazioni appropriate.
Esistono varie modalità di debridement; in base alle condizioni della ferita si procederà con quella più opportuna:
- Lo sbrigliamento autolitico si realizza attraverso l’applicazione di medicazioni a base di idrogeli , che hanno la funzione di ammorbidire e idratare necrosi e fibrina, stimolando così la dissoluzione dei tessuti morti. Una valida alternativa agli idrogeli sono i poliacrilati, i quali avendo una notevole compatibilità con i liquidi proteici (essudato), cedono gradualmente la soluzione (soluzione isotonica) di cui sono forniti e assorbono i liquidi essudati.
- Lo sbrigliamento meccanico prevede, invece, l’uso di forze fisiche, esercitate attraverso medicazioni “umide- secche”, che, aderendo al tessuto necrotico e ai detriti, li rimuovono.
- Lo sbrigliamento chirurgico dev’essere svolto esclusivamente dal medico ed è finalizzato ad un’eliminazione rapida di estese aree necrotiche.
- Il debridement enzimatico si basa sull’utilizzo di medicazioni a base di enzimi (collagenasi), che tagliano i legami peptilici presenti nel collagene e sono in grado di favorire l’allontanamento dei tessuti morti.
Ci sono situazioni in cui l’impiego della TPN può portare esiti clinici scarsi o addirittura eventi avversi. Uno dei principali è rappresentato dalla collocazione del dispositivo direttamente su organi o nervi esposti, siti anastomici, vasi sanguigni o tendini. In questo caso si potrebbe verificare l’erosione di queste strutture: sarà compito dell’infermiere dunque, controllare costantemente che non vi siano segni e sintomi di emorragia, valutando soprattutto le caratteristiche del fluido drenato nel canister e l’irrorazione distale, attraverso la palpazione dei polsi. Qualora la TPN fosse prescritta a pazienti con rischio conclamato di complicanze emorragiche, questi devono essere trattati e monitorati in un contesto assistenziale ritenuto appropriato dal medico curante. Bisogna fare particolare attenzione nel momento della rimozione della schiuma, perché può esserci il rischio di provocare un sanguinamento. E’ consigliabile dunque introdurre acqua sterile o soluzione salina sterile nella medicazione, attendere 15-30 minuti e poi rimuovere delicatamente la schiuma dalla ferita. È categoricamente sconsigliato utilizzare la NPT therapy in presenza di lesione di origine maligna, questo per evitare che si presenti la possibilità remota di proliferazione cangerogena. La TPN è controindicata anche in caso di osteomelite non trattata. In questi casi può essere opportuno rimuovere tutti i residui di tessuto necrotico, incluso l’osso infetto, (se necessario) e somministrare un’appropriata terapia antibiotica; infine proteggere l’osso intatto con un singolo strato di materiale non aderente.
Ci sono alcuni tipi di ferite per i quali la NPT therapy ha dimostrato apportare considerevoli benefici e queste sono:
- ferite acute/ traumatiche ;
- ferite addominali;
- ferite sternali;
- lesioni da decubito ;
- lesione degli arti inferiori;
- altre ferite chirurgiche ;
- fistole enteriche.
Generalmente le medicazioni sono utilizzate per favorire la guarigione delle ferite e prevenirne la contaminazione.
Per poter selezionare la medicazione più appropriata è necessario conoscere il tipo di materiale, che entra in contatto diretto con il letto della ferita, in quanto la selezione stessa deve tener conto di una serie di fattori, che definiscono la medicazione “ideale” per un tipo di ferita piuttosto che un altro.
Questi fattori rendono la ferita in grado di:
- permettere l’assorbimento dell’eccesso di essudato;
- creare un ambiente umido;
- rendere il sito sterile/pulito;
- non disperdere residui nella ferita;
- ridurre l’odore;
- essere di facile utilizzo;
- non essere allergica;
- non provocare traumi alla rimozione;
- fungere da barriera per i microrganismi;
- fornire un isolamento termico.
La scelta di una medicazione appropriata prevede la considerazione di più fattori quali:
- la tipologia della lesione,
- la sede,
- la dimensione,
- la presenza di infezione,
- il tipo,
- la quantità di essudato.
Successivamente hanno preso piede le medicazioni avanzate, che hanno caratteristiche di biocompatibilità: l’interazione della medicazione con il tessuto origina una risposta specifica.
Le medicazioni avanzate possono essere distinte in:
- “primarie”, quando il materiale della medicazione viene posto a diretto contatto con i tessuti lesi;
- “secondarie”, quando il materiale della medicazione serve per riempire una cavità o svolge la funzione di fissaggio della stessa.
Le medicazioni avanzate si possono dividere in quattro principali categorie, individuate in base alla loro azione:
- quelle che assorbono e trattengono i fluidi (idrocolloidi e schiume di poliuretano);
- quelle che assorbono solamente (granuli alginati e idrofibre);
- quelle che mantengono un ambiente umido (film di poliuretano);
- quelle che cedono i liquidi (idrogeli).
E’ stato dimostrato che l’ utilizzo della TPN contribuisce a ridurre le spese . Vari fattori concorrono a determinare il costo totale del trattamento della TPN:
- il tempo impiegato dell’assistenza infermieristica: sostituzione delle medicazioni, cura della ferita e della cute, valutazione e monitoraggio del processo di guarigione;
- l’aumento della necessità di cura: degenze prolungate, esami diagnostici più frequenti, intervento chirurgico, controllo del dolore;
- insorgenza di infezioni: somministrazione, su prescrizione, della terapia antibiotica, aumento del tempo dell’assistenza infermieristica e medica;
- costi legati ai prodotti impiegati per le medicazioni e alle apparecchiature;
- la percentuale di guarigione;
- l’impatto sull’ospedalizzazione ed eventi avversi.
Quando si svolge una valutazione dell’uso delle risorse è importante non concentrarsi esclusivamente sui costi unitari legati all’acquisto dei prodotti per le medicazioni, ma adottare una prospettiva più ampia che consenta di valutare l’uso complessivo delle risorse. Infatti, considerando che il solo acquisto di contenitore, tubi e noleggio domiciliare dell’apparecchio rispecchia una spesa di gran lunga superiore alle altre medicazioni, le aziende sanitarie generalmente propendono per l’abolizione del dispositivo, senza però considerare che la spesa maggiore, soprattutto nella cura delle ferite croniche, è rappresentata dal costo dell’assistenza infermieristica, dalle giornate di degenza e dalla gestione degli eventi avversi. Infatti, una medicazione che rimane in situ più a lungo consentirà di diminuire sia i costi relativi all’acquisto dei prodotti per la medicazione, che i costi legati all’assistenza infermieristica.
Per quanto riguarda, invece, gli aspetti organizzativi sarebbe auspicabile:
- la presenza in ogni azienda di un “case manager” (preferibilmente infermiere esperto in “wound care”) per la cura delle lesioni;
- la prescrizione della TPN riservata al medico dopo valutazione ;
- la realizzazione di “una presa in carico globale”, soprattutto per l’aspetto del monitoraggio
infermieristico della terapia; - l’ effettuazione della richiesta di TPN almeno 48 ore prima della dimissione o trasferimento del paziente ad altro livello assistenziale per non costituire ostacolo all’effettuazione di quest’ultima;
- la richiesta del consenso specifico al trattamento;
- la priorità del trattamento delle lesioni acute sulle croniche;
- la disponibilità dell’ attestazione preliminare della certificazione secondo la normativa
relativa alla sicurezza elettrica del device sia per il livello dell’ impiego ospedaliero che di quello domiciliare.
Si sottolinea che la diagnosi e la prescrizione della TPN , pertanto, è di competenza medica, mentre la gestione è di competenza infermieristica dopo aver acquisito competenze specifiche attraverso una formazione adeguata.
L’introduzione della terapia a pressione topica negativa ha creato nuove possibilità per la gestione di molte differenti tipologie di lesione.
Il trattamento della TPN comporta un cambiamento nella vita del paziente per cui un aspetto fondamentale di cui si dovrà occupare l’infermiere sarà sicuramente quello di individuare le esigenze e le preoccupazioni della persona, riconoscere e discutere i possibili ostacoli alla guarigione, fornire assistenza ricorrendo, dove necessario, ad altri specialisti, occupandosi così del paziente nel suo insieme. Alcune ricerche hanno evidenziato che la convivenza con lesioni di difficile guarigione spesso porta a dover affrontare una serie di problemi psicosociali ad esse strettamente correlati, che, se non adeguatamente affrontati e gestiti, possono indurre una risposta negativa al trattamento ed aggravare le difficoltà di guarigione. Infine valutando un trattamento con TPN therapy homecare è emerso come il paziente possa vivere in modo più positivo la situazione, qualora il nucleo familiare lo consentisse .L’ infermiere , pertanto, agisce in base alle proprie competenze e ricorre se necessario alla consulenza e all’ intervento di infermieri esperti o specialisti così come recita l’ art. 13 del codice deontologico del 2019 il quale dice che“L’Infermiere, agisce sulla base del proprio livello di competenza e ricorre, se necessario, alla consulenza e all’intervento di infermieri esperti o specialisti. Presta consulenza ponendo i suoi saperi e abilità a disposizione della propria e delle altre comunità professionali e istituzioni. Partecipa al percorso di cura e si adopera affinché la persona assistita disponga delle informazioni condivise con l’équipe, necessarie ai suoi bisogni di vita e alla scelta consapevole dei percorsi di cura proposti” .
Bibliografia.
- Armstrong DG, Attinger CE, Frykberg RG, Kirsner RS, Lavery LA, Mills JL: GuidelinesRegarding Negative Pressure Wound Therapy (NPWT) in the Diabetic Foot: Results of the Tucson Expert Consensun Conference (TECC) on V.A.C. Therapy. 2002.
Andrea Bellingeri – Il prontuario per la gestione delle lesioni cutanee – edizioni CdG, 2011 (nel documento Rizzella Tortona, infermiera specializzata). - B. M. Kostiuchenok, I. I. Kolker, V. A. Karlov, S. N. Ignatenko, and L. I. Muzykant, “Vacuum treatment in the surgical management of suppurative wounds,” Vestnik Khirurgii, vol. 137, no. 9, pp. 18–21, 1986.
- Davydov YA, Malafeeva AP, Smirnov AP. Vacuum therapy in the treatment of purulent lactation mastitis. Vestnik Khirurgii. 1986:9:66–70.
- European Wound Management Association (EWMA). Position Document: Management of wound infection. London: MEP Ltd, 2006.
- European Wound Management Association, documento di posizionamento: la pressione topica negativa nella gestione delle ferite, London: MEP Itd, 2007.
- European Wound Management Association (EWMA), Position Document: Wound bed preparation in practice. London: MEP ltd. 2004. 17. Wackenfors A, Sjögren J, Gustafsson R. Effects of vacuum- assisted closure therapy on inguinal wound edge microvascular blood flow. Wound Repair Regen 2004; 12(6): 600-06.
- Fleischmann W, Strecker W, Bombelli M, et al. Vacuum sealing as treatment of soft tissue damage in open fractures. Unfallchirurg 1993; 96(9): 488-92.
- Franks PJ, Posnett J, Cost- effectiveness of compression therapy. In European Wound Management Association (EWMA). Position Document: Understanding compression therapy. London, 2003: 8-10.
- Jones J. Winter’s concept of moist wound healing: a review of the evidence and impact on clinical practice. J Wound Care. 2005 Jun;14(6):273-6.
- Morykwas MJ, Argenta LC, Shelton-Brown EI, et al. Vacuum-assisted closure: a new method for wound control and treatment: animal studies and basic foundation. Ann Plast Surg 1997; 38(6): 553- 62.
- Nixon, J., Stoykova, B., Glanville, J.M., Drummond, M., Christie, J. And Kleijnen, J. (2000). The UK NHS Economic Evaluation Database: Economic Issues in evaluations of health thechnology. International Journal Of Public Health Thecnology Assessment. pp. 1-12. ISSN 1471-6348.
- Ozturk E, Ozguc H, Yilmazlar T. The use of vacuum assisted closure therapy in the management of Fournier’s gangrene, The American Journal of Surgery 2009; 197: 660-5.
- Persoon A, Heinen MM, van der Vleuten CJM, et al. Leg ulcers: a review of their impact on daily life. J Clin Nurs 2004; 13(3): 314-54.
- Vowden K. Conservative management of pressure ulcers. In: Banwell PE, Harding K (eds). Vacuum Assisted ClosureTM Therapy: Science and Practice. London: MEP Ltd, 2006. 12. Winter G. “Formation of scab and rate of epithelialization of superficial wound in 37 the skin of the young domestic pig” Nature, 1962.



[…] Gestione lesioni cutanee: la pressione negativa. proviene da AssoCareNews.it – Quotidiano Sanitario […]
[…] Gestione lesioni cutanee: la pressione negativa. proviene da AssoCareNews.it – Quotidiano Sanitario […]