Effetti della fluttuazione degli estrogeni durante il ciclo mestruale sulla risposta all’esercizio di accorciamento dello stretching nelle donne.
Oggi presentiamo uno studio realizzato dai ricercatori lituani Saulė Sipavičienė, Laura Daniusevičiutė, Irina Klizienė, Sigitas Kamandulis e Albertas Skurvydas sul tema “Effects of Estrogen Fluctuation during the Menstrual Cycle on the Response to Stretch-Shortening Exercise in Females“.
Lo scopo di questo studio era di indagare se la variazione dei livelli di estrogeni durante il ciclo mestruale influenza la suscettibilità al danno muscolare indotto dall’esercizio dopo l’esercizio del ciclo di accorciamento dello stretching. Donne fisicamente attive (; età = 20,2 ± 1,7 anni) hanno partecipato a questa ricerca. I soggetti hanno eseguito una sessione di 100 salti di caduta massimi il giorno 1 o 2 della fase follicolare e un’altra sessione identica il giorno 1 o 2 della fase ovulatoria; l’ordine delle sessioni è stato randomizzato. La coppia di picco del muscolo quadricipite femorale evocata dalla stimolazione elettrica e dalla contrazione volontaria massima, il dolore muscolare e l’attività CK sono stati misurati prima e in vari momenti fino a 72 ore dopo l’esercizio. È stato scoperto che l’alto livello di estrogeni durante la fase ovulatoria potrebbe essere correlato a un precedente ritorno alla forza muscolare di base dopo un intenso ciclo di allungamento accorciamento in quella fase rispetto alla fase follicolare. L’effetto estrogeno sembra essere altamente specifico per il sito danneggiato perché le differenze nella maggior parte dei marcatori EIMD (CK, dolore e affaticamento a bassa frequenza) tra le due fasi del ciclo mestruale erano piccole.
1. Introduzione.
Un carico fisico insolito e intenso o ad alto volume spesso produce danni muscolari indotti dall’esercizio (EIMD) e indolenzimento muscolare ritardato [1, 2]. Ciò è particolarmente comune quando si eseguono esercizi di ciclo di allungamento accorciamento che comportano l’allungamento di un muscolo attivo seguito da una rapida contrazione concentrica [3]. Il dolore e il gonfiore dei muscoli, l’aumento dell’attività della creatina chinasi (CK) plasmatica e il declino e il lento recupero della forza muscolare sono considerati marker indiretti dell’EIMD [4]. EIMD è stato segnalato in studi sia sull’uomo che sugli animali [1, 4–7].
Negli esseri umani, l’entità del danno muscolare varia da individuo a individuo e può essere spiegata da diversi fattori come il tipo e l’intensità dell’esercizio e l’età, il livello di forma fisica e il genotipo della persona [8-10]. Le differenze di sesso e, più precisamente, le differenze ormonali possono influenzare l’entità del danno e il recupero nei muscoli. La ricerca sui ratti ha suggerito che l’ormone femminile estrogeno influenza la riparazione post-EIMD del muscolo scheletrico attraverso l’attivazione delle cellule satellite [11]. A sostegno di questo concetto, le femmine mostrano meno danni muscolari rispetto ai maschi [7, 12]. Pertanto, si ritiene che gli ormoni sessuali possano influenzare l’entità del danno muscolare e il recupero dopo l’EIMD [13].
Contrariamente agli studi sugli animali, gli studi sugli esseri umani non hanno definito chiaramente l’effetto degli estrogeni sulla funzione contrattile muscolare e sull’EIMD [14]. Non esiste un’opinione uniforme e alcuni ricercatori sostengono che gli estrogeni non esercitano un effetto significativo sul danno muscolare dopo un carico fisico [15], mentre altri affermano che gli ormoni sessuali possono mitigare il danno muscolare e migliorare il recupero [13, 16]. Sebbene le differenze di sesso nell’EIMD siano state studiate su modelli animali, è stata eseguita una ricerca insufficiente sugli esseri umani. La maggior parte delle ricerche sulle differenze di sesso nell’affaticamento muscolare e nel recupero non ha preso in considerazione le fasi del ciclo mestruale, durante le quali i livelli di estrogeni fluttuano notevolmente [7, 17, 18]. Sebbene i dati degli studi sull’uomo siano contraddittori [19, 20], i risultati degli studi sugli animali ci portano a ipotizzare che si verificherebbe un minor danno muscolare dopo un carico fisico e che il recupero muscolare sarebbe più veloce durante la fase del ciclo mestruale con la più alta concentrazione di estrogeni.
Lo scopo di questo studio era di indagare se la variazione del livello di estrogeni durante il ciclo mestruale influenza la suscettibilità di una donna all’EIMD in risposta all’esercizio del ciclo di accorciamento dello stiramento. Poiché i livelli di estrogeni differiscono in modo significativo tra le prime fasi follicolari e ovulatorie del ciclo mestruale [17], abbiamo confrontato le risposte all’esercizio di accorciamento dello stretching eseguito durante queste due fasi.
2. Materiale e metodi.
2.1. Partecipanti.
Hanno partecipato a questa ricerca donne sane e fisicamente attive (n. 18; età = 20,2 ± 1,7 anni; peso = 56,2 ± 4,1 kg; altezza = 167,3 ± 3,2 cm) che non utilizzavano la contraccezione ormonale e con un ciclo mestruale regolare. Per valutare le fasi del ciclo mestruale, la temperatura rettale è stata registrata ogni mattina prima di alzarsi dal letto per tre mesi consecutivi. L’inizio della fase follicolare era indicato dall’inizio delle mestruazioni e l’inizio dell’ovulazione era indicato da un aumento della temperatura di 0,5 ° C. Il protocollo di ricerca è stato discusso e approvato dal Comitato Etico della Ricerca Biomedica Regionale di Kaunas. Prima dell’inizio dell’indagine, ogni soggetto ha letto e firmato un modulo di consenso informato scritto e il protocollo dello studio era coerente con i principi delineati nella Dichiarazione di Helsinki.
2.2. Esecuzione del carico di esercizio del ciclo di allungamento accorciamento.
Ogni soggetto ha eseguito 100 salti di caduta massimi da un’altezza di 0,75 m da una piattaforma con un rimbalzo massimo immediato su una piastra di forza Kistler (tipo 9286A, Amherst, NY, USA). I salti sono stati eseguiti con un contromovimento a un angolo di 90 ° nel ginocchio a un intervallo di 20 s. Durante l’esecuzione dei salti, il soggetto ha posto le mani in vita. I soggetti sono stati informati dell’altezza di ogni salto e sono stati motivati a eseguire ogni salto il più in alto possibile. È stata registrata l’altezza di tutti i salti e la differenza tra il più alto dei 10 salti iniziali e il più alto dei 10 salti finali è stata utilizzata come indicatore della fatica indotta dal ciclo di allungamento accorciamento.
2.3. Coppia isometrica e stimolazione elettrica.
La coppia isometrica è stata misurata nei muscoli estensori del ginocchio utilizzando un dinamometro isocinetico (System 3; Biodex Medical Systems, Shirley, NY, USA). La stimolazione muscolare diretta è stata applicata utilizzando tre elettrodi di gomma carbonizzata ricoperti da un sottile strato di gel per elettrodi (ECG-EEG Gel; Medigel, Modi’in, Israel). Due degli elettrodi (6 × 10 cm) sono stati posizionati trasversalmente lungo la larghezza della porzione prossimale del quadricipite femorale. Il terzo elettrodo (6 × 10 cm) copriva la porzione distale del muscolo sopra la rotula. È stato utilizzato uno stimolatore elettrico standard (MG 440; Medicor, Budapest, Ungheria). La stimolazione elettrica è stata erogata in impulsi ad onda quadra della durata di 1 ms. La tolleranza dei volontari alla stimolazione elettrica è stata valutata in un’occasione separata e tutti i partecipanti che sono stati reclutati per lo studio hanno mostrato una buona compliance con la procedura. L’intensità della stimolazione elettrica è stata selezionata individualmente applicando un singolo stimolo ai muscoli testati. Durante la stimolazione elettrica, la gamba è stata fissata con un angolo del ginocchio di 90 ° (0 ° = estensione completa del ginocchio). Le misurazioni includevano la coppia massima di contrazione isometrica volontaria (MVC) e la coppia evocata nei quadricipiti da treni di 1 s di stimolazione elettrica a 20 Hz (P20) e 100 Hz (P100). Le procedure per la stimolazione elettrica erano essenzialmente le stesse descritte in precedenza [21].
2.4. Attività di CK al plasma.
Circa 5 ml di sangue sono stati prelevati dalla vena cubitale mediana da personale medico esperto. I campioni sono stati centrifugati immediatamente e analizzati per l’attività CK utilizzando un analizzatore biochimico Spotchem EZ SP-4430 (Menarini Diagnostics, Winnersh-Wokingham, UK) con strisce reagenti morbide (ARKRAY Factory, Inc., Shiga, Giappone).
2.5. Concentrazione di estrogeni nel sangue.
All’inizio di ogni esperimento, è stato prelevato un campione di 5 mL di sangue venoso per misurare la concentrazione di estrogeni (17β-estradiolo) nel sangue. Il sangue è stato analizzato utilizzando l’analisi dell’elettrochemiluminescenza e gli analizzatori immunologici Roche Elecsys 1010/2010 Cobas e 411 e Modular Analytics E170 (Roche Diagnostics GmbH, Germania).
2.6. Dolore muscolare.
La gravità del dolore del quadricipite è stata valutata soggettivamente dai soggetti dopo 2-3 squat utilizzando una scala da 0 a 10 punti. Questo metodo di valutazione del dolore muscolare è stato utilizzato in studi precedenti [6, 22].
2.7. Procedura sperimentale.
Una settimana prima della ricerca, i soggetti conoscevano il corso dell’esperimento e gli veniva insegnato come eseguire l’esercizio. I soggetti hanno eseguito il protocollo sperimentale due volte: (1) una sessione il giorno 1 o 2 della fase follicolare e (2) un’altra sessione il giorno 1 o 2 della fase ovulatoria. L’ordine di queste sessioni è stato randomizzato e l’intervallo di tempo tra le sessioni è stato di almeno 10 settimane per minimizzare la potenziale manifestazione di effetti ripetuti [23]. Il giorno dell’esperimento in entrambe le fasi, è stato prelevato un campione di sangue venoso per la misurazione della concentrazione del 17β-estradiolo e dell’attività CK. Il soggetto ha eseguito un riscaldamento di corsa sul posto a bassa intensità per 5 min, dopodiché si è seduta sulla sedia del dinamometro Biodex. Durante il test, il soggetto ha eseguito un MVC e il picco di coppia di una contrazione involontaria del muscolo quadricipite femorale è stato evocato dalla stimolazione elettrica a frequenza di 20 Hz e 100 Hz. Il soggetto ha quindi eseguito un ciclo di allenamento per accorciare lo stiramento per evocare il danno al muscolo quadricipite femorale (come descritto sopra). La forza muscolare è stata misurata di nuovo a 2 minuti e 24, 48 e 72 ore dopo l’allenamento. Il dolore muscolare è stato valutato a 24, 48 e 72 ore e l’attività CK a 24 ore dopo l’allenamento.
2.8. Analisi statistica.
Abbiamo calcolato la media aritmetica e la deviazione standard per ogni variabile. La normalità della distribuzione dei dati è stata verificata e confermata dal test di Kolmogorov-Smirnov. È stata utilizzata un’analisi della varianza a due vie (ANOVA) per misure ripetute per determinare gli effetti della fase mestruale (fase follicolare rispetto a fase ovulatoria) e del tempo (dopo 2 minuti e 24, 48 e 72 ore di recupero) sulle proprietà misurate in muscolo quadricipite. Se è stato riscontrato un effetto significativo, è stato eseguito un test post hoc per individuare le differenze tra le medie applicando test accoppiati con una correzione di Bonferroni per confronti multipli. Le variazioni di altezza di salto, attività CK e indolenzimento muscolare sono state analizzate da test accoppiati. La significatività è stata fissata a P <0,05.
3.1. Valori iniziali.
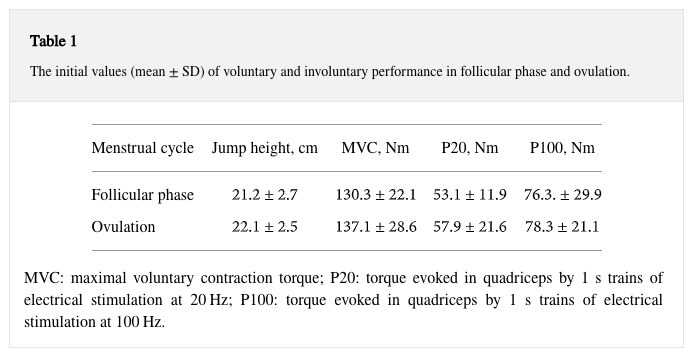
La concentrazione di 17β-estradiolo era significativamente più alta nella fase ovulatoria rispetto alla fase follicolare (229,6 +- 81.8 pmol/L contro 119 +- 61,7 pmol / L, P < 0,05). Tuttavia, la MVC e la coppia di contrazione muscolare indotta elettricamente non differivano tra le fasi (P < 0,05, Tabella 1).
3.2. Esercizio sul ciclo di accorciamento dello stretching.
L’altezza del salto è diminuita durante l’esercizio in entrambe le fasi del ciclo mestruale. Confrontando il miglior tentativo dei 10 salti iniziali con i 10 salti finali, l’altezza è diminuita del 14,5 +- 3,5% nella fase follicolare e del 9,1 +- 2.1% nella fase ovulatoria (P > 0,05).
3.3. Forza muscolare.
L’MVC e la coppia di estensione del ginocchio indotta elettricamente sono diminuiti in modo significativo immediatamente dopo l’esercizio del ciclo di accorciamento dell’allungamento in entrambe le fasi mestruali (P < 0,05 rispetto al rispettivo livello iniziale, P > 0,05 tra le fasi, Figure 1, 2 e 3).
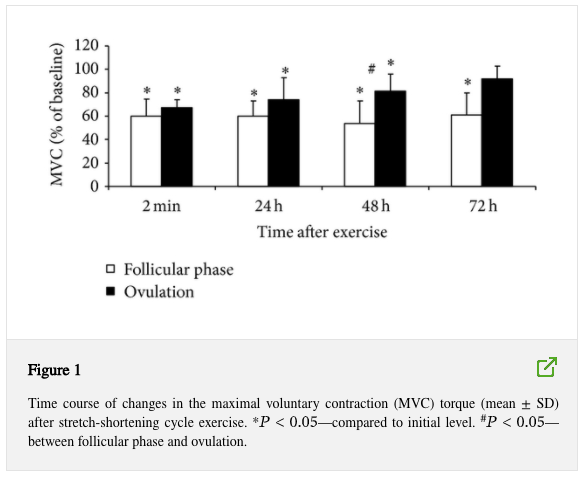
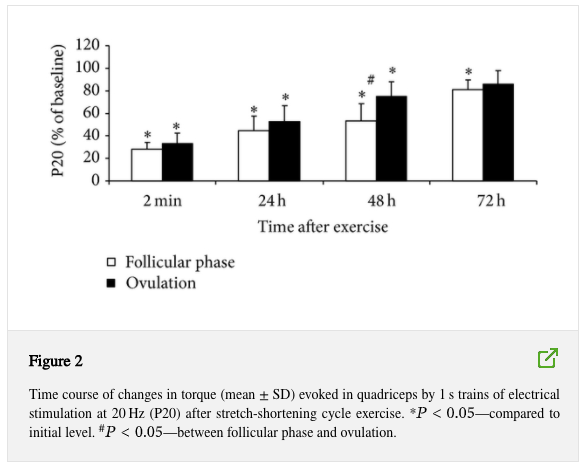
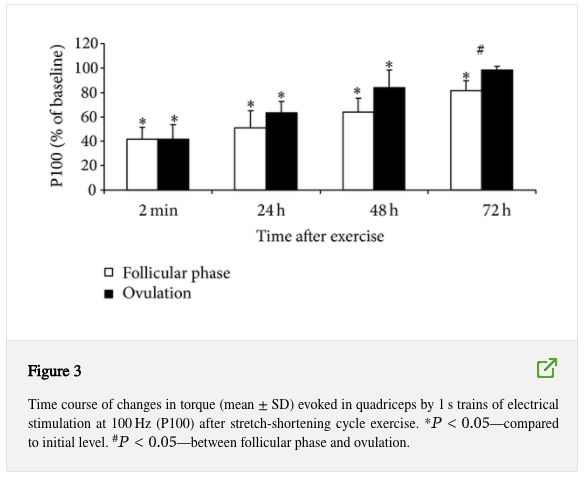
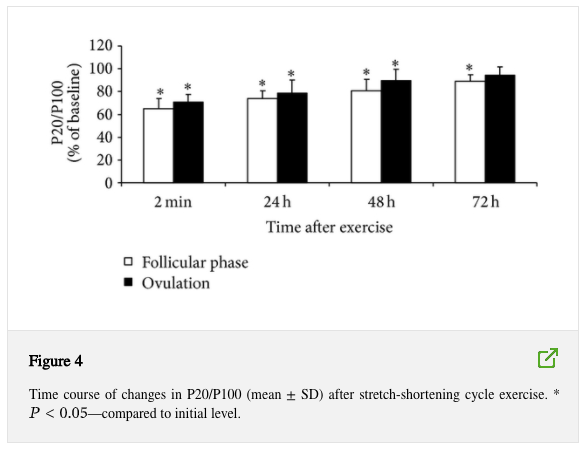
MVC e P100 misurati 48 e 72 ore dopo l’esercizio erano inferiori nella fase ovulatoria rispetto alla fase follicolare (P < 0,05). P20 non differiva tra le fasi. MVC, P20 e P100 si sono ripresi completamente a 72 ore dopo l’esercizio nella fase ovulatoria, ma sono rimasti ridotti in questo momento nella fase follicolare (rispetto al livello iniziale). Il rapporto P20 / P100 è diminuito in entrambe le condizioni (P < 0,05) ma non differiva tra le condizioni in nessun momento (Figura 4).
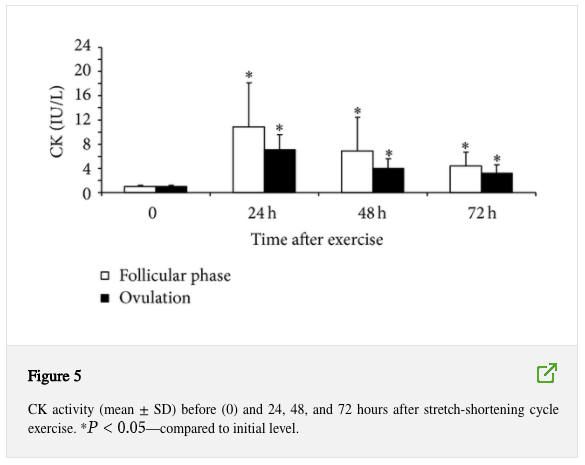
3.4. Attività CK e dolore muscolare.
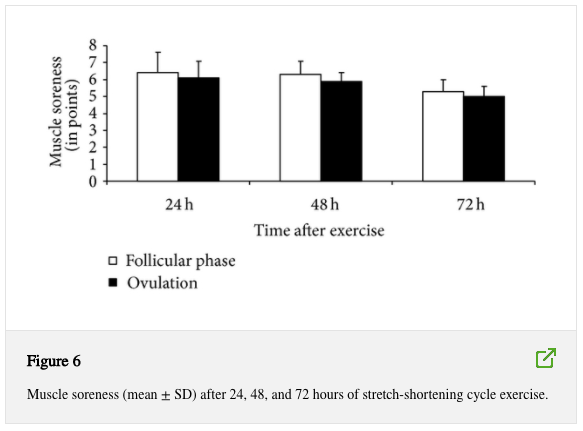
Dopo l’esercizio del ciclo di allungamento accorciamento, l’attività CK è aumentata a un livello simile in entrambe le fasi (P < 0,05 rispetto al rispettivo livello iniziale, P > 0,05 tra le fasi, Figura 5). L’indolenzimento muscolare non differiva tra le due fasi in nessun momento dopo l’esercizio (P < 0,05, Figura 6).
4. Discussione.
I risultati di questa ricerca dimostrano due punti. In primo luogo, gli indicatori indiretti di danno muscolare, come la diminuzione della MVC, i momenti di estensione del ginocchio indotti elettricamente e l’affaticamento a bassa frequenza misurati immediatamente dopo l’esercizio del ciclo di accorciamento dell’allungamento, non differivano tra le fasi della fase mestruale. In secondo luogo, il recupero della forza muscolare del quadricipite era maggiore nella fase ovulatoria rispetto alla fase follicolare, mentre l’affaticamento a bassa frequenza, l’attività CK e il dolore muscolare non differivano tra le fasi.
EIMD. Le condizioni sperimentali utilizzate in questo studio sembravano causare EIMD da moderata a grave, come dimostrato dalla grande riduzione della capacità di generazione della forza, specialmente con la stimolazione a bassa frequenza (> 70%), dolore muscolare (6-7 punti su 10) e aumento di 5-6 volte dell’attività della CK plasmatica. La diminuzione della forza muscolare immediatamente dopo l’esercizio del ciclo di accorciamento dell’allungamento non sembra essere correlata all’accumulo di metaboliti, come fosfato e ioni idrogeno, nel miooplasma perché è improbabile che i salti di caduta eseguiti a intervalli di 20 s inducano cambiamenti significativi di energia metaboliti [24]. Inoltre, la riduzione della forza muscolare è rimasta evidente per almeno 2 giorni di recupero, che sono troppo lunghi perché i metaboliti influiscano sulla funzione muscolare. I cambiamenti osservati nelle prestazioni muscolari a seguito dell’esercizio di accorciamento dell’allungamento possono riflettere cambiamenti strutturali negli elementi contrattili e citoscheletrici all’interno delle fibre muscolari. Tali anomalie strutturali nel muscolo dopo l’esercizio eccentrico possono includere dischi Z irregolari, miofilamenti disorganizzati e sarcomeri ipercontratti o tesi [1, 25]. I cambiamenti strutturali possono anche riflettere il rimodellamento della struttura miofibrillare [26, 27].
Sono state osservate riduzioni maggiori della coppia evocata a 20 Hz rispetto alla stimolazione muscolare a 100 Hz, indicando la presenza di affaticamento a bassa frequenza dopo 100 salti (Figura 4). La diminuzione della coppia muscolare evocata dalla stimolazione a bassa frequenza riflette una diminuzione della concentrazione di ioni Ca2 + scaricati dal reticolo sarcoplasmatico e la sensibilità delle miofibrille agli ioni Ca2 + [28]. A causa delle differenze nelle dinamiche di accoppiamento eccitazione-contrazione, è probabile che la coppia muscolare evocata dalla stimolazione ad alta frequenza cambi meno di quella evocata dalla stimolazione a bassa frequenza [29, 30]. La fatica a bassa frequenza osservata nel presente studio può riflettere un fallimento nell’accoppiamento eccitazione-contrazione.
Effetto ciclo mestruale. I dati confermano in parte le ipotesi della nostra ricerca secondo cui, ad alte concentrazioni di estrogeni, l’EIMD immediatamente dopo un intenso esercizio fisico potrebbe essere meno grave e il recupero muscolare potrebbe essere più rapido. In questi soggetti, il grado simile di compromissione della funzione muscolare (ad esempio, diminuzione della coppia e dell’altezza del salto) immediatamente dopo il salto suggerisce una quantità simile di danno indotto da un intenso ciclo di allungamento e accorciamento (Figure 1-3). Questi risultati contrastano con i risultati osservati durante il periodo di recupero, quando la forza muscolare è tornata al livello iniziale prima nella fase ovulatoria rispetto alla fase follicolare. Questa differenza suggerisce fortemente che specifici cambiamenti funzionali del ciclo mestruale sono correlati all’effetto degli estrogeni sui meccanismi di rigenerazione muscolare e che la rigenerazione dopo EIMD può essere associata alla risposta infiammatoria all’esercizio che danneggia i muscoli. Alcune ricerche sugli animali hanno dimostrato che gli estrogeni influenzano direttamente l’infiammazione e che gli estrogeni riducono l’infiltrazione dei leucociti nei muscoli dopo un nuovo esercizio [7, 9]. La prevenzione dell’infiltrazione leucocitaria da parte di estrogeni può limitare il danno e provocare un più rapido recupero muscolare. I muscoli possono riprendersi dall’EIMD più velocemente nelle donne a causa dei loro livelli di estrogeni più elevati e di una reazione infiammatoria più debole [15, 31]. Tuttavia, questo particolare effetto degli estrogeni deve ancora essere documentato nell’uomo [31].
L’infiltrazione nei muscoli dei leucociti (soprattutto dei macrofagi), che attivano le cellule satelliti, è essenziale per la rigenerazione muscolare [32, 33]. Pertanto, la prevenzione dell’infiltrazione dei leucociti nei muscoli può rallentare fasi importanti nel processo di rigenerazione muscolare [7]. L’infiammazione può anche diminuire il danno muscolare riducendo la produzione di fattori ossidanti. Ad esempio, gli estrogeni possono influenzare l’attività dell’ossido nitrico sintasi inducibile (iNOS) e la sintesi induttiva di iNOS in più tessuti e possono quindi influenzare l’entità del danno e il recupero dei muscoli dopo l’esercizio [34]. Gli estrogeni rilasciati in risposta al danno muscolare scheletrico possono anche influenzare i processi infiammatori e di rigenerazione muscolare influenzando la produzione di iNOS nelle cellule satellite all’interno dei muscoli [9, 11].
Anche se il rilascio di CK dai muscoli non è un indicatore diretto del danno alla struttura muscolare, è considerato un indicatore adeguato di ridotta stabilità della membrana cellulare muscolare [4]. L’aumentata permeabilità del sarcolemma associata al danno muscolare consente alla CK di uscire dai muscoli e apparire nel flusso sanguigno [35]. Gli estrogeni sono potenti antiossidanti che funzionano come stabilizzatori di membrana interagendo con il doppio strato fosfolipidico della membrana [9]. Queste qualità antiossidanti degli estrogeni potrebbero mitigare il danno muscolare dopo un carico fisico [13]. Non abbiamo esaminato se l’entità del danno alla membrana cellulare muscolare associata all’EIMD cambia durante il ciclo mestruale. Sebbene l’attività di CK fornisca una stima dell’entità del danno, i cambiamenti nell’attività di CK dovrebbero essere interpretati con cautela perché il livello di CK può essere influenzato dalla velocità di rimozione dal flusso sanguigno [36] o dalla precedente esposizione a esercizi di tipo eccentrico [22 ].
Dopo carichi fisici eccentrici eccessivi, le cellule danneggiate rilasciano bradichinina, istamina e prostaglandine, che aumentano la sensibilità dei recettori del dolore e contribuiscono a ritardare il dolore e la sensibilità muscolare [37]. Il dolore compare comunemente insieme ad altri sintomi tipici del processo infiammatorio come rigidità muscolare, gonfiore e sensibilità alla palpazione [4]. Nel presente studio è stato osservato anche dolore muscolare, ma non differiva in modo significativo tra le fasi del ciclo mestruale. Coerentemente con i cambiamenti nel dolore muscolare, i cambiamenti nell’affaticamento a bassa frequenza erano indipendenti dal livello di estrogeni nel presente studio. Ciò suggerisce che l’effetto mediato dagli estrogeni era insufficiente per produrre cambiamenti nell’indolenzimento muscolare e nei meccanismi di generazione della fatica a bassa frequenza.
Il presente studio indica che l’aumento del livello di estrogeni influisce sul processo di rigenerazione muscolare e migliora la funzione muscolare durante la fase ovulatoria. Tuttavia, notiamo che altri fattori importanti oltre agli estrogeni (ad esempio, la distribuzione dei liquidi e la termoregolazione) possono influenzare il recupero dopo il carico fisico durante le diverse fasi mestruali [17]. La mancanza di un modello sperimentale “gold standard” è una limitazione in tutti gli studi sull’uomo degli effetti degli estrogeni sulla funzione muscolare.
5. Conclusioni.
Il presente studio dimostra che la forza muscolare ritorna al livello di base più velocemente dopo un intenso ciclo di allungamento accorciamento durante la fase ovulatoria, quando il livello di estrogeni è alto, rispetto alla fase follicolare. L’effetto estrogeno sembra essere altamente specifico per il sito danneggiato perché le differenze nella maggior parte dei marker EIMD (CK, dolore e fatica a bassa frequenza) tra le due fasi del ciclo mestruale erano piccole.
Conflitto d’interessi.
Gli autori dichiarano di non avere conflitti di interessi.
Ringraziamenti.
Il presente studio è stato sostenuto da sovvenzioni del Consiglio lituano della ricerca.
Bibliografia.
- F. Lauritzen, G. Paulsen, T. Raastad, L. H. Bergersen, and S. G. Owe, “Gross ultrastructural changes and necrotic fiber segments in elbow flexor muscles after maximal voluntary eccentric action in humans,” Journal of Applied Physiology, vol. 107, no. 6, pp. 1923–1934, 2009.View at: Publisher Site | Google Scholar
- K. Nosaka, M. Newton, and P. Sacco, “Muscle damage and soreness after endurance exercise of the elbow flexors,” Medicine and Science in Sports and Exercise, vol. 34, no. 6, pp. 920–927, 2002.View at: Google Scholar
- P. V. Komi, “Physiological and biomechanical correlates of muscle function: effects of muscle structure and stretch-shortening cycle on force and speed,” Exercise and Sport Sciences Reviews, vol. 12, pp. 81–121, 1984.View at: Google Scholar
- G. L. Warren, D. A. Lowe, and R. B. Armstrong, “Measurement tools used in the study of eccentric contraction-induced injury,” Sports Medicine, vol. 27, no. 1, pp. 43–59, 1999.View at: Publisher Site | Google Scholar
- G. Paulsen, U. R. Mikkelsen, T. Raastad, and J. M. Peake, “Leucocytes, cytokines and satellite cells: what role do they play in muscle damage and regeneration following eccentric exercise?” Exercise Immunology Review, vol. 18, pp. 42–97, 2012.View at: Google Scholar
- A. Skurvydas, M. Brazaitis, T. Venckunas, and S. Kamandulis, “Predictive value of strength loss as an indicator of muscle damage across multiple drop jumps,” Applied Physiology, Nutrition and Metabolism, vol. 36, no. 3, pp. 353–360, 2011.View at: Publisher Site | Google Scholar
- P. M. Tiidus, “Oestrogen and sex influence on muscle damage and inflammation: evidence from animal models,” Current Opinion in Clinical Nutrition and Metabolic Care, vol. 4, no. 6, pp. 509–513, 2001.View at: Publisher Site | Google Scholar
- P. M. Clarkson and M. J. Hubal, “Are women less susceptible to exercise-induced muscle damage?” Current Opinion in Clinical Nutrition and Metabolic Care, vol. 4, no. 6, pp. 527–531, 2001.View at: Publisher Site | Google Scholar
- D. L. Enns and P. M. Tiidus, “The influence of estrogen on skeletal muscle: sex matters,” Sports Medicine, vol. 40, no. 1, pp. 41–58, 2010.View at: Publisher Site | Google Scholar
- T. Venckunas, A. Skurvydas, M. Brazaitis, S. Kamandulis, A. Snieckus, and C. N. Moran, “Human alpha-actinin-3 genotype association with exercise-induced muscle damage and the repeated-bout effect,” Applied Physiology, Nutrition, and Metabolism, vol. 37, pp. 1038–1046, 2012.View at: Google Scholar
- D. L. Enns and P. M. Tiidus, “Estrogen influences satellite cell activation and proliferation following downhill running in rats,” Journal of Applied Physiology, vol. 104, no. 2, pp. 347–353, 2008.View at: Publisher Site | Google Scholar
- P. M. Tiidus, D. Holden, E. Bombardier, S. Zajchowski, D. Enns, and A. Belcastro, “Estrogen effect on post-exercise skeletal muscle neutrophil infiltration and calpain activity,” Canadian Journal of Physiology and Pharmacology, vol. 79, no. 5, pp. 400–406, 2001.View at: Publisher Site | Google Scholar
- P. M. Tiidus, “Influence of estrogen on skeletal muscle damage, inflammation, and repair,” Exercise and Sport Sciences Reviews, vol. 31, no. 1, pp. 40–44, 2003.View at: Publisher Site | Google Scholar
- K. A. Sewright, M. J. Hubal, A. Kearns, M. T. Holbrook, and P. M. Clarkson, “Sex differences in response to maximal eccentric exercise,” Medicine and Science in Sports and Exercise, vol. 40, no. 2, pp. 242–251, 2008.View at: Publisher Site | Google Scholar
- N. Stupka, S. Lowther, K. Chorneyko, J. M. Bourgeois, C. Hogben, and M. A. Tarnopolsky, “Gender differences in muscle inflammation after eccentric exercise,” Journal of Applied Physiology, vol. 89, no. 6, pp. 2325–2332, 2000.View at: Google Scholar
- P. M. Wise, D. B. Dubal, M. E. Wilson, S. W. Rau, and M. Böttner, “Minireview: neuroprotective effects of estrogen—new insights into mechanisms of action,” Endocrinology, vol. 142, no. 3, pp. 969–973, 2001.View at: Publisher Site | Google Scholar
- X. A. K. Janse de Jonge, “Effects of the menstrual cycle on exercise performance,” Sports Medicine, vol. 33, no. 11, pp. 833–851, 2003.View at: Publisher Site | Google Scholar
- J. Kaikkonen, E. Porkkala-Sarataho, T. P. Tuomainen et al., “Exhaustive exercise increases plasma/serum total oxidation resistance in moderately trained men and women, whereas their VLDL + LDL lipoprotein fraction is more susceptible to oxidation,” Scandinavian Journal of Clinical and Laboratory Investigation, vol. 62, no. 8, pp. 599–608, 2002.View at: Publisher Site | Google Scholar
- S. C. Chung, A. H. Goldfarb, A. Z. Jamurtas, S. S. Hegde, and J. Lee, “Effect of exercise during the follicular and luteal phases on indices of oxidative stress in healthy women,” Medicine and Science in Sports and Exercise, vol. 31, no. 3, pp. 409–413, 1999.View at: Google Scholar
- M. H. Joo, E. Maehata, T. Adachi, A. Ishida, F. Murai, and N. Mesaki, “The relationship between exercise-induced oxidative stress and the menstrual cycle,” European Journal of Applied Physiology, vol. 93, no. 1-2, pp. 82–86, 2004.View at: Publisher Site | Google Scholar
- A. Skurvydas, S. Kamandulis, and N. Masiulis, “Two series of fifty jumps performed within sixty minutes do not exacerbate muscle fatigue and muscle damage,” Journal of Strength and Conditioning Research, vol. 24, no. 4, pp. 929–935, 2010.View at: Publisher Site | Google Scholar
- S. Kamandulis, A. Skurvydas, A. Snieckus et al., “Monitoring markers of muscle damage during a 3 week periodized drop-jump exercise programme,” Journal of Sports Sciences, vol. 29, no. 4, pp. 345–353, 2011.View at: Publisher Site | Google Scholar
- K. Nosaka, M. J. Newton, and P. Sacco, “Attenuation of protective effect against eccentric exercise-induced muscle damage,” Canadian Journal of Applied Physiology, vol. 30, no. 5, pp. 529–542, 2005.View at: Google Scholar
- K. Sahlin and J. M. Ren, “Relationship of contraction capacity to metabolic changes during recovery from a fatiguing contraction,” Journal of Applied Physiology, vol. 67, no. 2, pp. 648–654, 1989.View at: Google Scholar
- L. Féasson, D. Stockholm, D. Freyssenet et al., “Molecular adaptations of neuromuscular disease-associated proteins in response to eccentric exercise in human skeletal muscle,” Journal of Physiology, vol. 543, no. 1, pp. 297–306, 2002.View at: Publisher Site | Google Scholar
- C. Malm, “Exercise-induced muscle damage and inflammation: fact or fiction?” Acta Physiologica Scandinavica, vol. 171, no. 3, pp. 233–239, 2001.View at: Publisher Site | Google Scholar
- J. G. Yu, L. Carlsson, and L. E. Thornell, “Evidence for myofibril remodeling as opposed to myofibril damage in human muscles with DOMS: an ultrastructural and immunoelectron microscopic study,” Histochemistry and Cell Biology, vol. 121, no. 3, pp. 219–227, 2004.View at: Publisher Site | Google Scholar
- D. G. Allen, G. D. Lamb, and H. Westerblad, “Skeletal muscle fatigue: cellular mechanisms,” Physiological Reviews, vol. 88, no. 1, pp. 287–332, 2008.View at: Publisher Site | Google Scholar
- J. S. Nielsen, K. Madsen, L. V. Jørgensen, and K. Sahlin, “Effects of lengthening contraction on calcium kinetics and skeletal muscle contractility in humans,” Acta Physiologica Scandinavica, vol. 184, no. 3, pp. 203–214, 2005.View at: Publisher Site | Google Scholar
- H. Westerblad, S. Duty, and D. G. Allen, “Intracellular calcium concentration during low-frequency fatigue in isolated single fibers of mouse skeletal muscle,” Journal of Applied Physiology, vol. 75, no. 1, pp. 382–388, 1993.View at: Google Scholar
- P. M. Tiidus, “Can oestrogen influence skeletal muscle damage, inflammation, and repair?” British Journal of Sports Medicine, vol. 39, no. 5, pp. 251–253, 2005.View at: Publisher Site | Google Scholar
- J. E. Anderson and A. C. Wozniak, “Satellite cell activation on fibers: modeling events in vivo—an invited review,” Canadian Journal of Physiology and Pharmacology, vol. 82, no. 5, pp. 300–310, 2004.View at: Publisher Site | Google Scholar
- T. J. Hawke, “Muscle stem cells and exercise training,” Exercise and Sport Sciences Reviews, vol. 33, no. 2, pp. 63–68, 2005.View at: Publisher Site | Google Scholar
- F. S. Laroux, K. P. Pavlick, I. N. Hines et al., “Role of nitric oxide in inflammation,” Acta Physiologica Scandinavica, vol. 173, no. 1, pp. 113–118, 2001.View at: Publisher Site | Google Scholar
- S. P. Sayers and P. M. Clarkson, “Short-term immobilization after eccentric exercise. Part II: creatine kinase and myoglobin,” Medicine and Science in Sports and Exercise, vol. 35, no. 5, pp. 762–768, 2003.View at: Publisher Site | Google Scholar
- P. M. Clarkson, E. P. Hoffman, E. Zambraski et al., “ACTN3 and MLCK genotype associations with exertional muscle damage,” Journal of Applied Physiology, vol. 99, no. 2, pp. 564–569, 2005.View at: Publisher Site | Google Scholar
- B. Kendall and R. Eston, “Exercise-induced muscle damage and the potential protective role of estrogen,” Sports Medicine, vol. 32, no. 2, pp. 103–123, 2002.View at: Google Scholar
Leggi anche:
Ciclo Mestruale: capire come funziona aiuta a gestirlo meglio.
Stretching: cos’è, a cosa serve e quali tipi di allungamento muscolare esistono?



[…] Fluttuazione degli estrogeni durante il Ciclo Mestruale su risposta accorciamento stretching nelle d… proviene da AssoCareNews.it – Quotidiano Sanitario […]
[…] Fluttuazione degli estrogeni durante il Ciclo Mestruale su risposta accorciamento stretching nelle d… proviene da AssoCareNews.it – Quotidiano Sanitario […]
[…] Fluttuazione degli estrogeni durante il Ciclo Mestruale su risposta accorciamento stretching nelle d… proviene da AssoCareNews.it – Quotidiano Sanitario […]